心理所研究發現內側前額葉皮質小膠質細胞和TNFα功能不足介導青少期社會應激誘導的認知靈活性損傷
青少期階段是抑郁癥、精神分裂癥、成癮行為等一些常見精神疾病高發和易感的階段。這一階段的各種負性社會經歷是其發生發展的重要誘發因素。盡管這些疾病表現出各種不同的癥狀表型,其中前額葉皮質介導的執行功能障礙被認為是共同的主要癥狀之一。同伴欺侮是青少群體常見的社會應激源。利用 “居留者-入侵者”社會挫敗模型誘發嚙齒類動物類似的應激經歷,通過以前的研究發現青少期階段的應激暴露能夠誘導小鼠成年后前額葉皮質介導的認知靈活性明顯受損(圖1)。認知靈活性是一種隨著環境變化對目標導向行為進行相應調整的高級腦功能。這種能力在抑郁癥、精神分裂癥、創傷后應激障礙等多種精神疾病患者中表現出不同程度的損害,并與疾病預后和藥物治療反應密切相關。
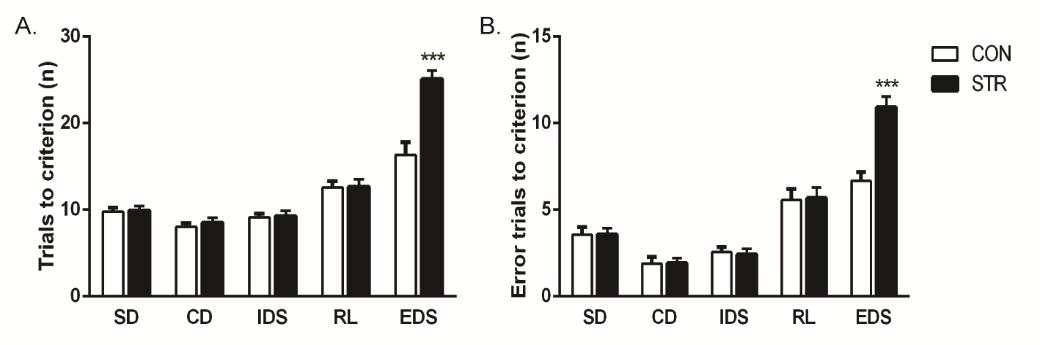
圖1 青少期社會應激誘導成年期小鼠認知靈活性損傷
傳統研究多從神經元的角度探討認知功能障礙的神經機制,認為應激導致的神經元/突觸聯結強度或可塑性的改變是其重要的病理生理基礎。近年來的研究表明,腦內主要的免疫細胞-小膠質細胞(Microglia),通過分泌一系列的化學因子和免疫因子與神經元交互作用,共同調節腦發育、神經可塑性及其介導的認知功能。值得注意的是,出生后腦內小膠質細胞及其釋放的因子的表達、分布和功能呈現出動態發展變化,對神經環路的形成、維系和重塑十分重要。然而,目前對于青少期社會應激如何影響免疫細胞和相關分子,以及這種影響與認知功能障礙之間的關系所知甚少。
研究發現,伴隨認知靈活性損傷的同時,青少期社會應激誘導該行為介導腦區內側前額葉皮質(mPFC)的小膠質細胞及其釋放的一種細胞因子腫瘤壞死因子α(TNFα)的功能不足,主要表現為小膠質細胞數量減少、一級突起長度縮短和其特異性的結構標記分子—離子鈣接頭蛋白1(Iba1)表達降低(見圖2),以及TNFα在mRNA和蛋白水平上的表達均降低(見圖3)。通過直接給予健康成年小鼠mPFC慢性微注射TNFα中和劑抑制其作用,造成了類似的認知靈活性的選擇性損害(見圖4)。成年期急性小劑量LPS免疫激活(見圖5)和慢性抗抑郁藥物反苯環丙胺(TCP)治療(見圖6),都有效逆轉了青少期社會應激誘導的認知靈活性損傷,并恢復了mPFC受抑制的小膠質細胞和TNFα活動水平。
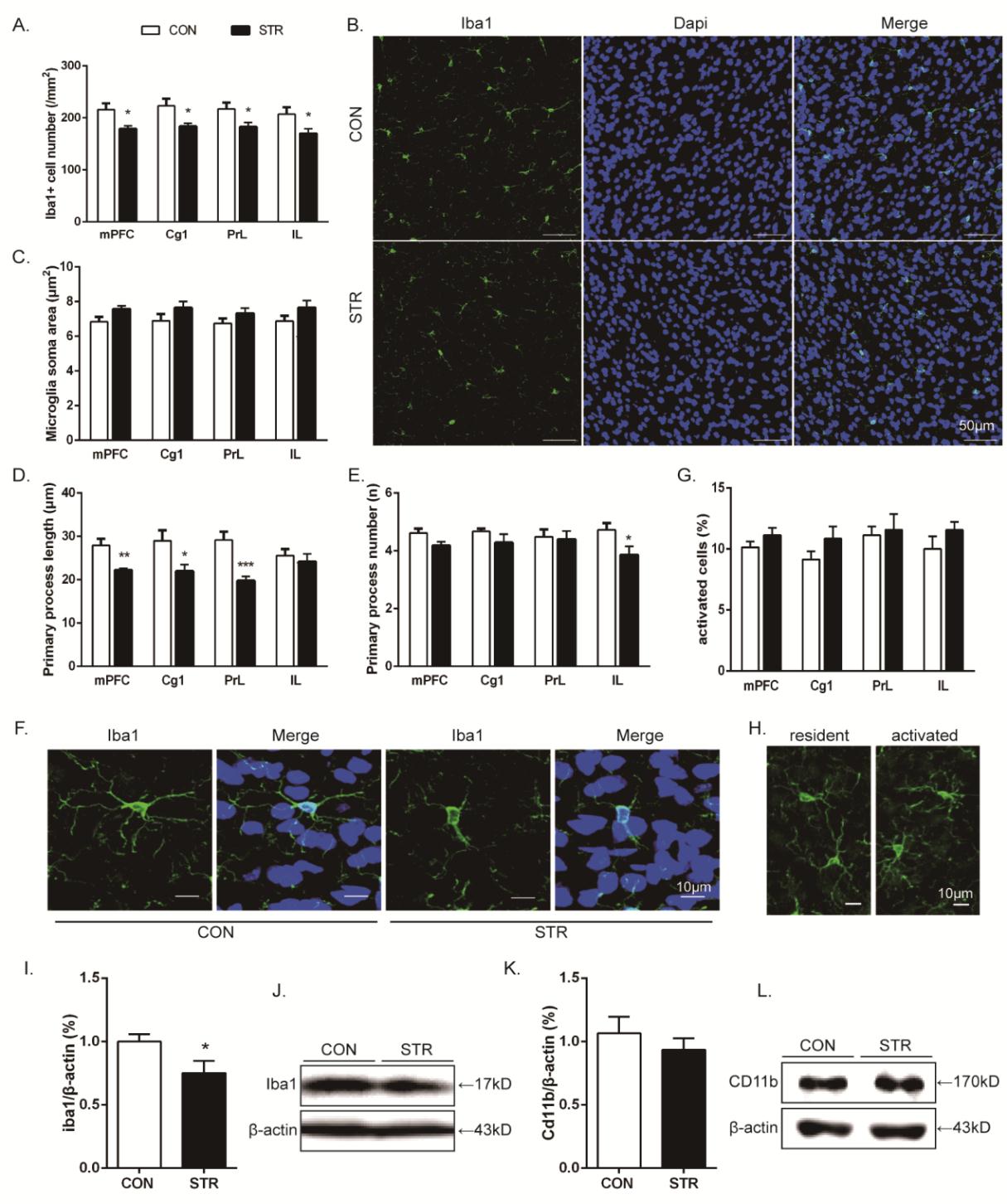
圖2 青少期社會應激誘導成年小鼠mPFC小膠質細胞功能不足
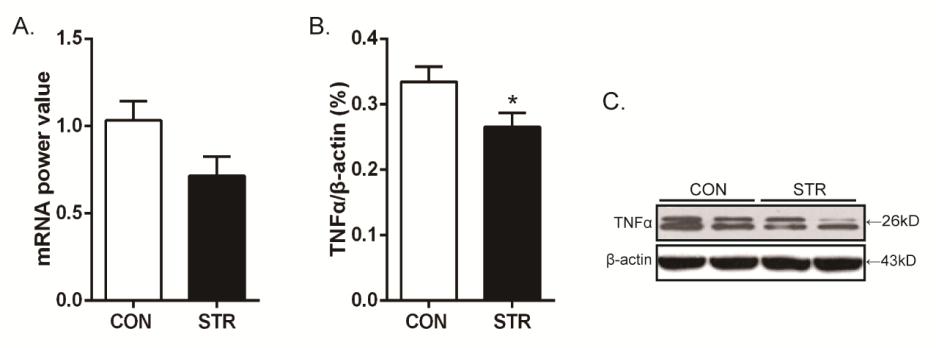
圖3 青少期社會應激降低成年小鼠mPFC TNFα mRNA和蛋白水平
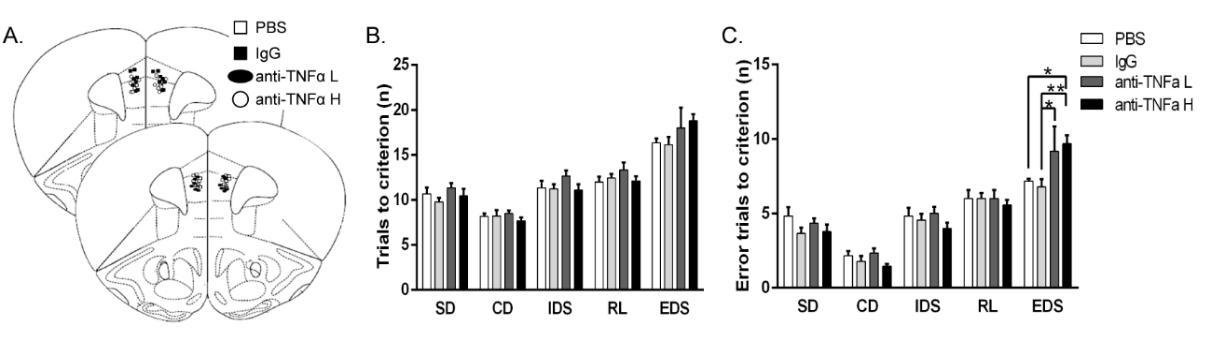
圖4 成年健康小鼠mPFC慢性微注射TNFα中和劑選擇性損害認知靈活性
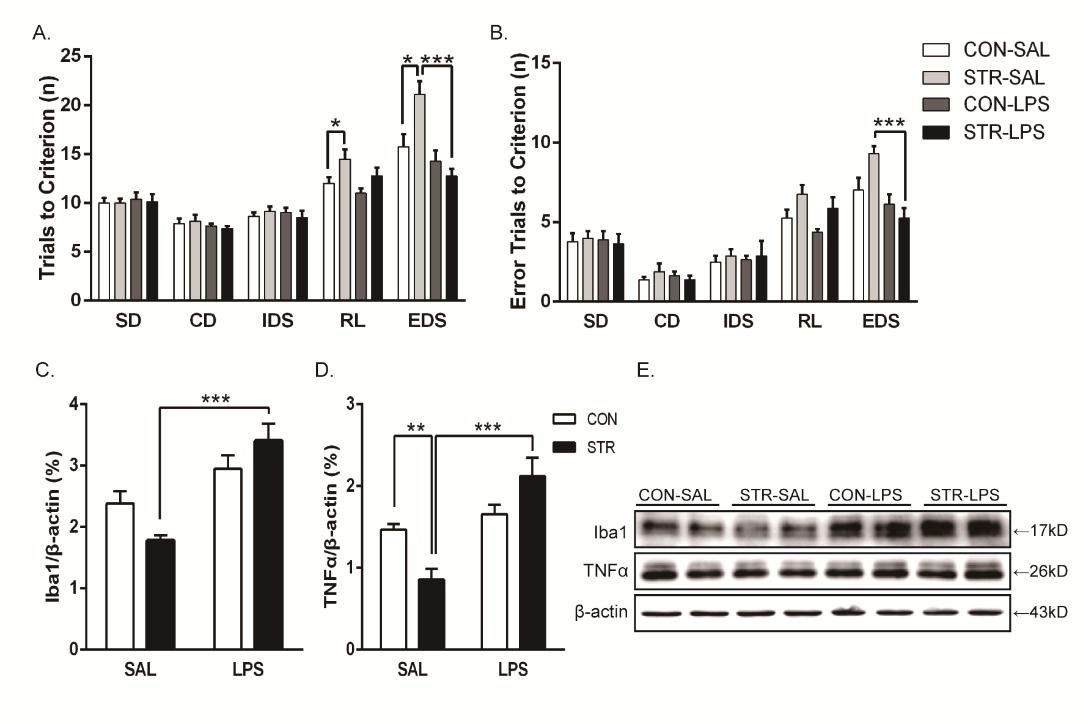
圖5 成年期急性LPS免疫激活逆轉了青少期社會應激誘導的認知靈活性損傷,恢復了mPFC受抑制的小膠質細胞和TNFα活動水平

圖6 成年期慢性抗抑郁藥物TCP治療逆轉了青少期社會應激誘導的認知靈活性損傷,恢復了mPFC受抑制的小膠質細胞和TNFα活動水平
這些研究結果提示了一種以前未知的小膠質細胞和TNFα在認知功能調節中的重要作用,為建立基于免疫調節的精神疾病相關認知功能障礙治療的新策略提供了潛在靶點。
該研究受國家自然科學基金(31771217; 81471122)和中國科學院心理健康重點實驗室基金資助。文章已在線發表于Brain, behavior, and immunity。
論文信息:
Zhang, Y., Xu, H., Zhang, F., Shao, F., Ellenbroek, B., Wang, J., et al. (2019). Deficiency of microglia and TNFα in the mPFC-mediated cognitive inflexibility induced by social stress during adolescence. Brain, behavior, and immunity,
https://doi.org/10.1016/j.bbi.2019.1002.1010.
附件下載:

