心理所研究揭示慢波睡眠期間記憶重激活的“回聲”效應
記憶在大腦中的存儲與演化是一個復雜且動態的過程,其中一些記憶能夠隨著時間的推移而愈發清晰,而另一些則逐漸模糊甚至消失。這一現象長期以來吸引了科學界的廣泛關注,研究者們致力于揭示其背后的神經機制。目前,科學界普遍認為,慢波睡眠在記憶的鞏固和演化過程中扮演著關鍵角色。具體而言,新形成的記憶最初存儲在海馬體中,隨后在睡眠期間通過記憶重激活的方式逐漸轉移到新皮層,從而形成更為穩定的長期記憶。這一轉移過程被認為是記憶鞏固的核心機制之一。
盡管已有研究表明,睡眠期間的記憶重激活是記憶鞏固的重要環節,但海馬體與新皮層在這一過程中的動態交互機制仍不明確。理解這兩者之間的相互作用對于全面揭示記憶鞏固的神經機制至關重要。然而,迄今為止,尚未有研究對這一關鍵問題展開深入探討。
為探究這一問題,中國科學院心理研究所王亮研究組開展了一項研究,探索海馬體與新皮層在記憶重激活中的協同作用,以及這一過程如何受到睡眠階段、神經振蕩等因素的調控。該研究不僅有助于深化對記憶鞏固機制的理解,還可能為記憶相關疾病的治療提供新的思路。

該研究結合人類顱內腦電技術(intracranial EEG)與目標記憶重激活范式(Targeted Memory Reactivation, TMR),探討了記憶重激活期間海馬體與皮層的神經活動特征與信息交互模式。研究揭示了慢波睡眠期間目標記憶通過多次重激活機制增強記憶鞏固的神經機制,并闡明了記憶再激活過程中海馬尖波漣漪、皮層紡錘波以及海馬-皮層神經交互作用的動態時空特征。
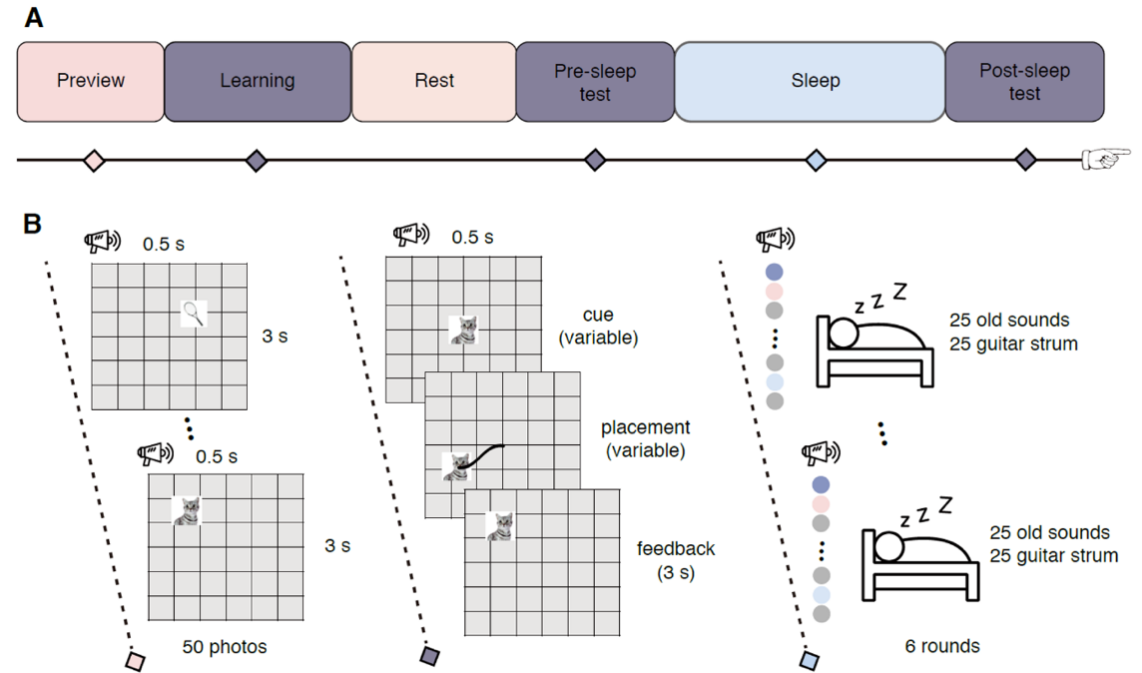
圖1. 實驗流程圖
研究團隊采用TMR實驗范式,在學習物體-位置關聯任務后的慢波睡眠階段,通過播放特定聲音線索重新激活記憶內容(圖1)。同時,研究人員通過記錄藥物難治性癲癇患者的顱內腦電信號,同時監測海馬和皮層的電生理活動,通過分析學習-睡眠之間腦活動模式的相似性衡量記憶的重激活強度(圖2)。
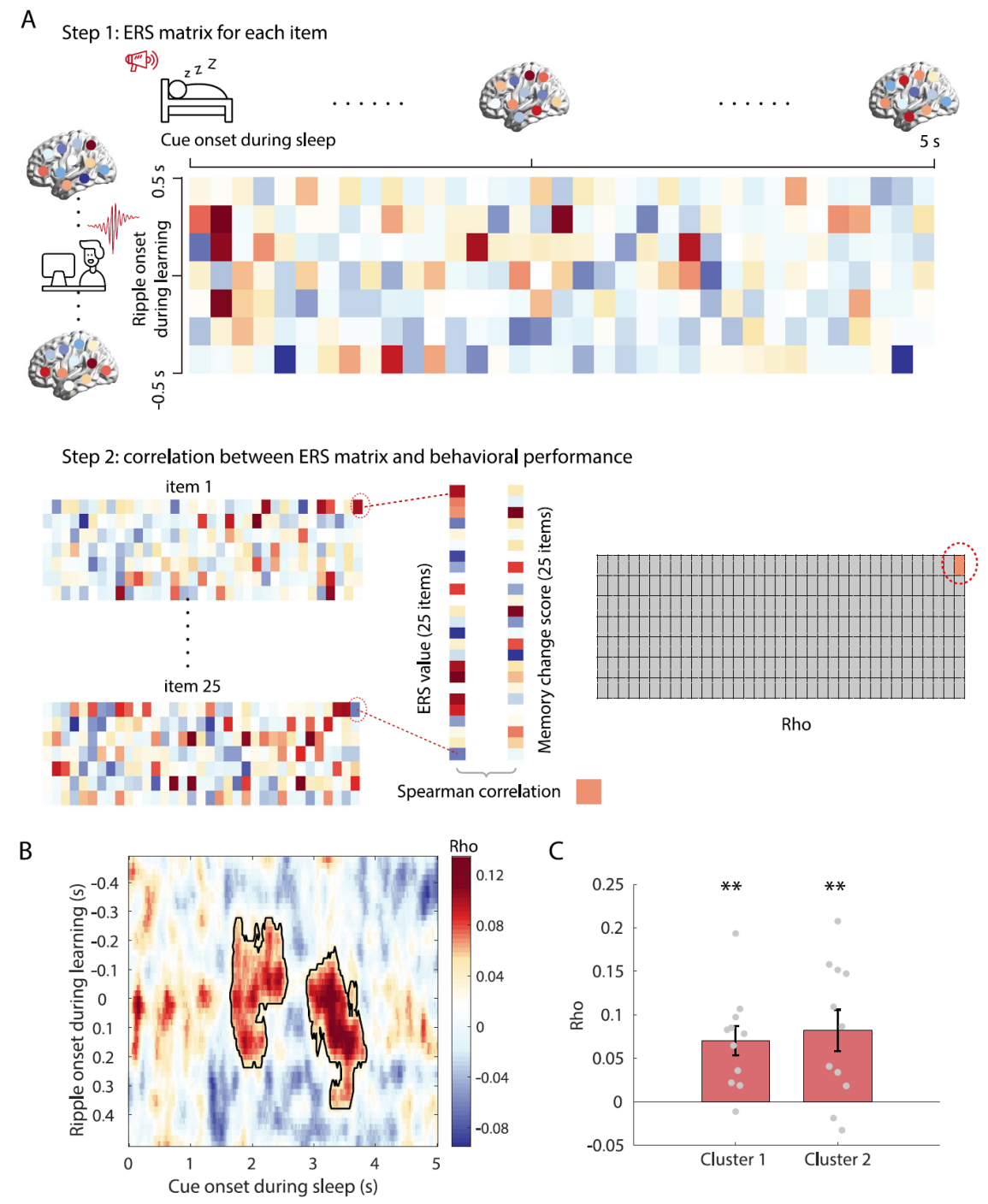
圖2.?睡眠中的多次記憶重激活
研究者發現,在慢波睡眠期間播放聲音刺激之后,記憶信息會出現兩次分離的重激活現象(圖2),第一次發生在聲音播放之后的1.6到2.6秒,第二次發生在2.8到3.8秒。這一結果表明,深度睡眠期間的記憶鞏固可能需要多次重激活。這種現象好比記憶信息在大腦中以慢波振蕩的節奏產生的“回聲”,其原因可能是因為皮層和海馬之間需要通過多次的信息處理來實現記憶的鞏固。那么,海馬和新皮層的活動是否在第一次重激活和第二次的“回聲”之間有區別呢?
海馬尖波漣漪活動(ripple)和皮層紡錘波活動(spindle)在記憶固中非常重要,這兩種特征波形的產生往往代表著記憶信息的整合加工。因此,研究者接下來分析了兩次重激活之間,海馬尖波漣漪和皮層紡錘波活動的具體情況(圖3)。結果發現,第一次重激活期間,記憶增強組的海馬尖波漣漪活動顯著增強,而在第二次重激活期間確沒有此現象。與此相反,記憶增強組的皮層紡錘波活動在第一次重激活期間并沒有變化,而是在第二次重激活期間顯著增強。

圖3.?慢波睡眠期間海馬尖波漣漪和皮層紡錘波
研究者進一步探究了海馬-皮層同步性在兩次再激活過程中的動態信息交互(圖4)。結果表明,在第一次重激活過程中,記憶增強組海馬-皮層的連通性顯著增強,而在第二次重激活時連通性下降。這種海馬-皮層連通性的反轉效應可能反映了海馬與皮層在記憶重激活早期的耦合和隨后的解耦合對記憶鞏固的促進作用。
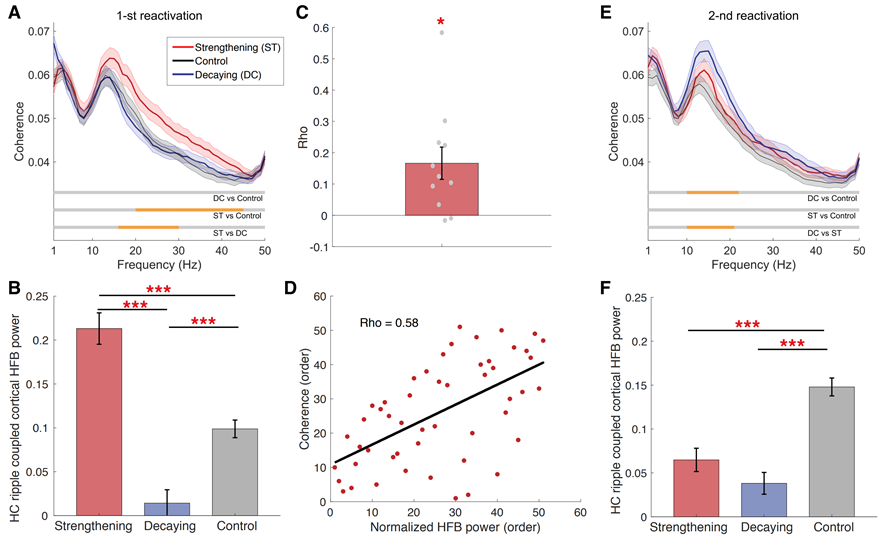
圖4.?慢波睡眠期間海馬-皮層的動態信息交互
基于上述結果,研究團隊提出了一種動態模型來描述慢波睡眠期間記憶鞏固的過程(圖5)。慢波睡眠期間播放的聲音線索會誘發多次的皮層重激活,而且在重激活發生期間通過皮層和海馬之間交替的耦合與去耦合選擇性促進記憶鞏固。具體表現為,第一次重激活期間,海馬通過功能連接和跨腦區耦合的高頻神經振蕩與皮層進行交互,在第二次重激活期間,皮層和海馬發生去耦合,此時皮層獨立處理記憶信息,表現為皮層紡錘波活動的增強。
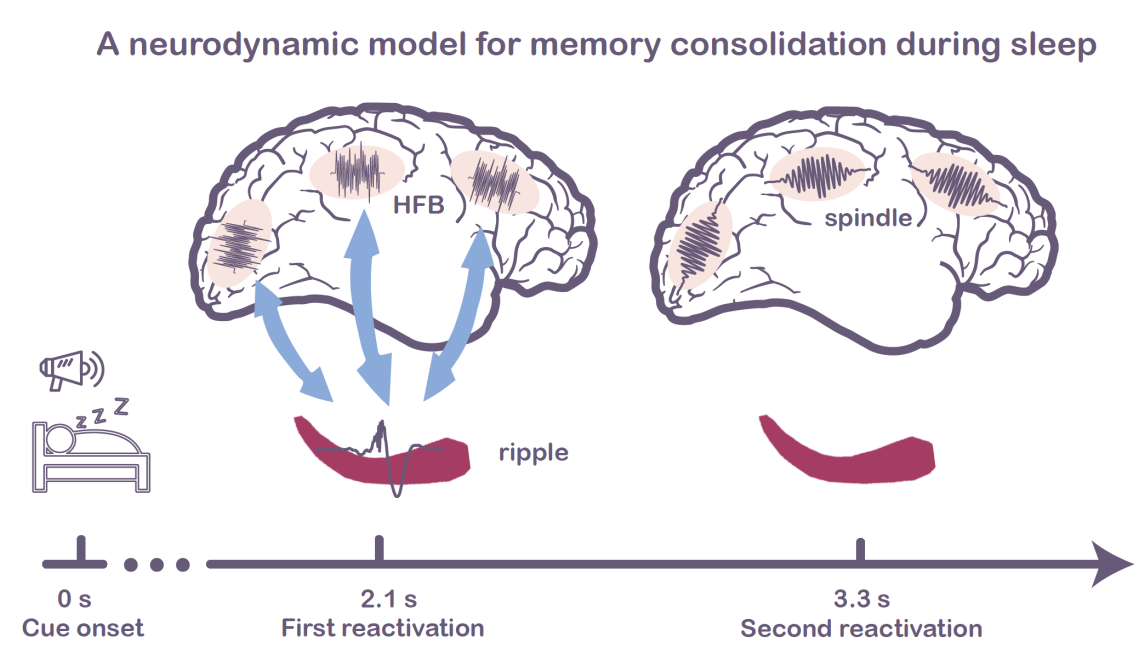
圖5.?睡眠中選擇性記憶鞏固的神經動力學模型
該研究獲得基金委重點國際合作項目(32020103009)和科技創新2030重大項目(2022ZD0205000)的資助。
相關成果已在線發表于Nature Communications。心理所博士研究生段威和天津師范大學心理學院徐戰勝博士為論文共同第一作者,心理所王亮研究員為論文的通訊作者。心理所陳棟副研究員,已畢業學生劉佳麗、譚政、肖雪和在讀博士生呂鵬程,北京三博腦科醫院王靜主任和王夢陽主任,美國西北大學Ken Paller教授和德國波鴻魯爾大學Nikolai Axmacher教授為該研究做出重要貢獻。
論文信息:
Duan W#, Xu Z#, Chen D, Wang J, Liu J, Tan Z, Xiao X, Lv P, Wang M, Paller K A, Axmacher N, Wang L*. Electrophysiological signatures underlying variability in human memory consolidation. Nat Commun, 2025, 16(1): 2472.?https://doi.org/10.1038/s41467-025-57766-x
附件下載:

