心理所研究揭示疼痛敏感性個體差異的神經生物標記物
疼痛敏感性存在很大的個體差異:同一個疼痛刺激對某人而言可能痛得無法忍受,但對另一個人而言卻可能完全不痛。這一個體差異的神經基礎為何是疼痛領域的核心問題之一。這一問題雖然早已受到疼痛研究者的關注[1],但至今仍未得到明確的解答,最近兩項100人左右的研究甚至得出了完全相反的結論[2-3]。
近期,中國科學院心理研究所胡理研究組開展了一項大樣本研究,利用總樣本量達1046的六個功能磁共振數據集(圖1),系統探究了腦激活是否可反映疼痛敏感性個體差異這一問題,并開發了一個高度可泛化的疼痛敏感性神經生物標記物。
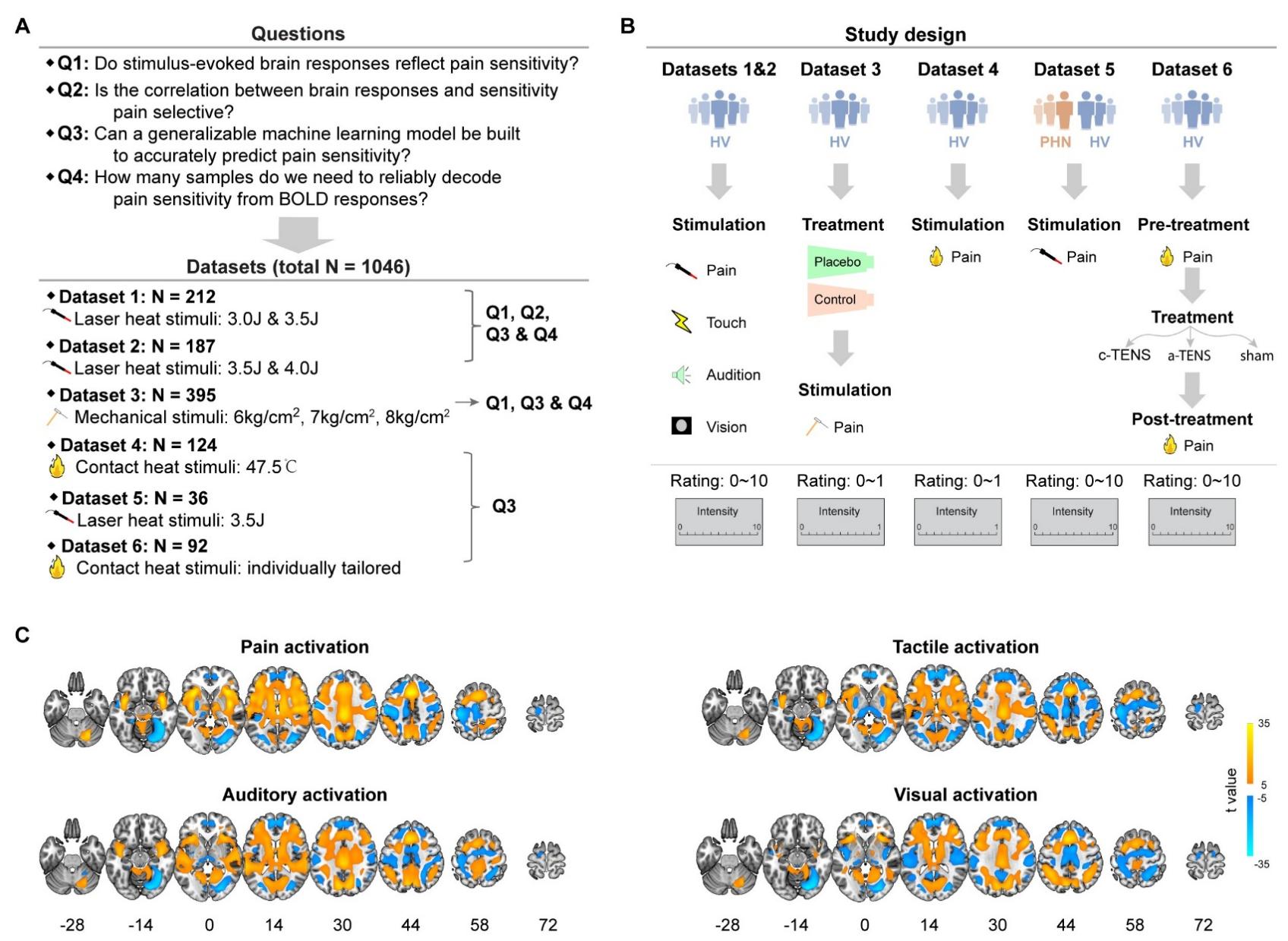
圖1. 研究問題、數據集和實驗設計概況
研究團隊首先分析了自主采集的大樣本功能磁共振數據集,發現疼痛刺激誘發的腦激活與疼痛敏感性存在顯著相關,這一結果在另一個大樣本數據集中也得到了很好的重復(圖2A、2B)。研究團隊進一步利用重采樣的方法,發現了樣本量對腦激活與疼痛敏感性的相關有很大影響,即便樣本量達到210,也只有25%的體素和疼痛敏感性的關系能夠被穩定檢驗出來(圖2C)。這說明以往樣本量100左右的研究仍可能不具有充足的統計檢驗力,因而得出了相互矛盾的結果。
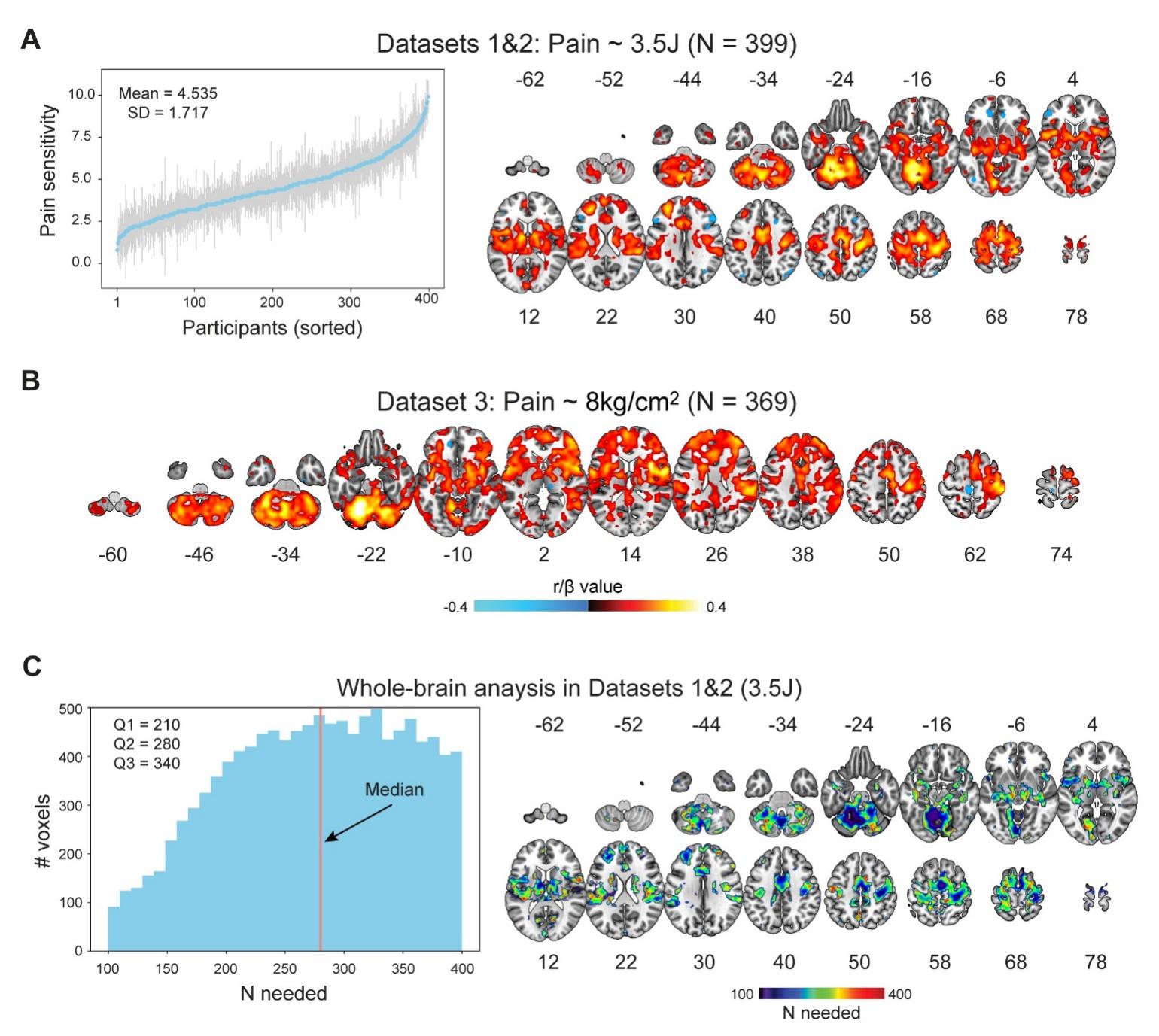
圖2. 腦激活反映疼痛敏感性個體差異
接著,研究團隊通過對非痛刺激誘發腦激活的分析,發現腦激活和非痛感覺敏感性個體差異也存在相關,但這一相關明顯弱于腦激活和疼痛敏感性的相關。這說明腦激活和感覺敏感性個體差異的關系并非是疼痛特異的,但腦激活對疼痛敏感性的編碼具有一定的偏向性。
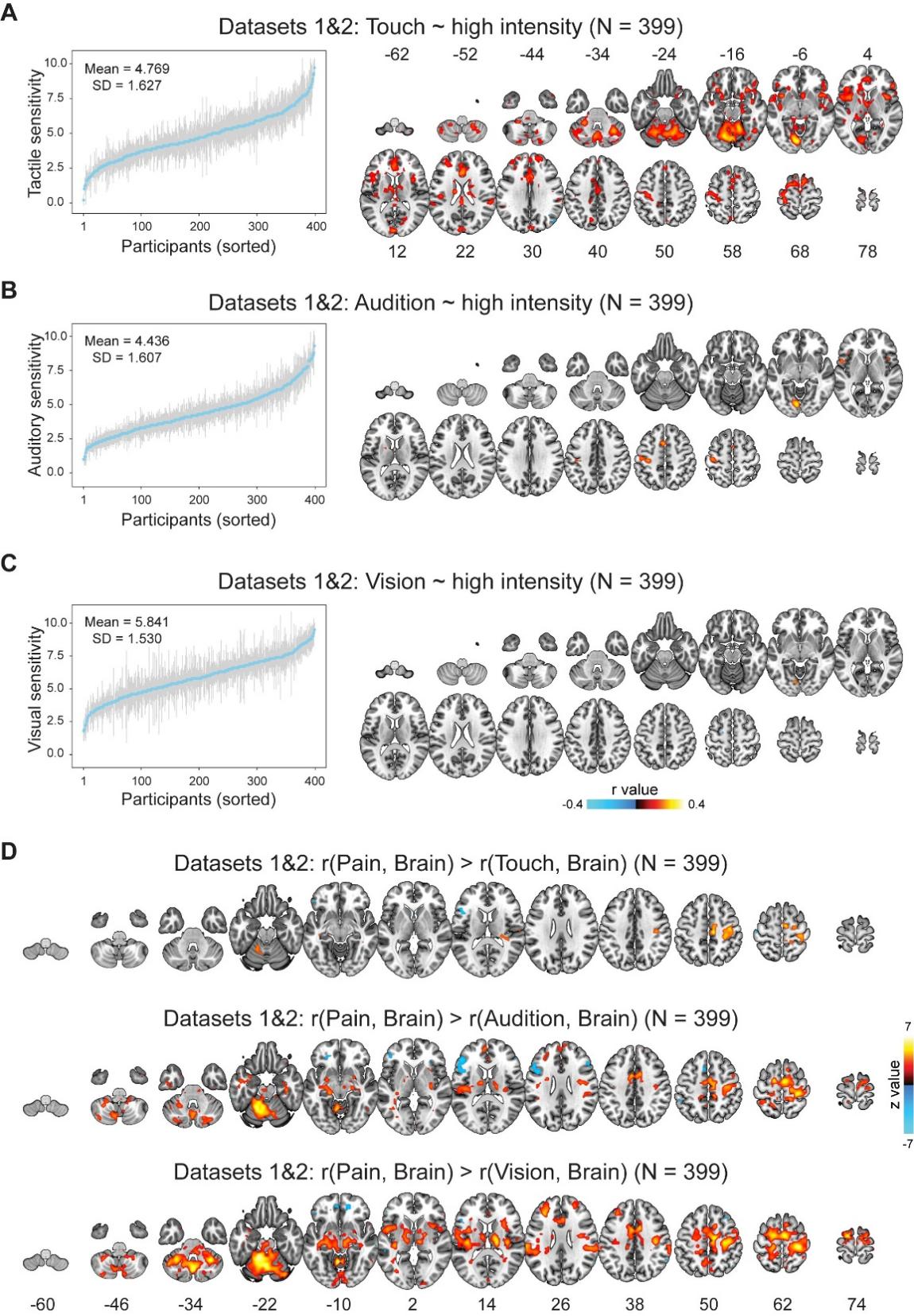
圖3. 腦激活對疼痛敏感性的編碼具有偏向性
基于上述研究結果,研究團隊利用機器學習技術開發了一個疼痛敏感性預測模型(Neuroimaging-based Indicator of Pain Sensitivity [NIPS])。該模型在激光熱痛、接觸式熱痛、機械誘發痛中均顯示出對疼痛敏感性的顯著預測能力(圖4)。不僅如此,NIPS還能預測帶狀皰疹后遺神經痛(PHN)患者的疼痛敏感性。通過對比NIPS和經典疼痛預測模型[4-5],研究團隊發現只有NIPS在所有數據集中都顯著預測疼痛敏感性。更值得關注的是,NIPS甚至可以預測安慰劑和經皮神經電刺激的鎮痛作用(圖4D)。這些結果證明NIPS具有高度可泛化性,且具備潛在的臨床應用價值。
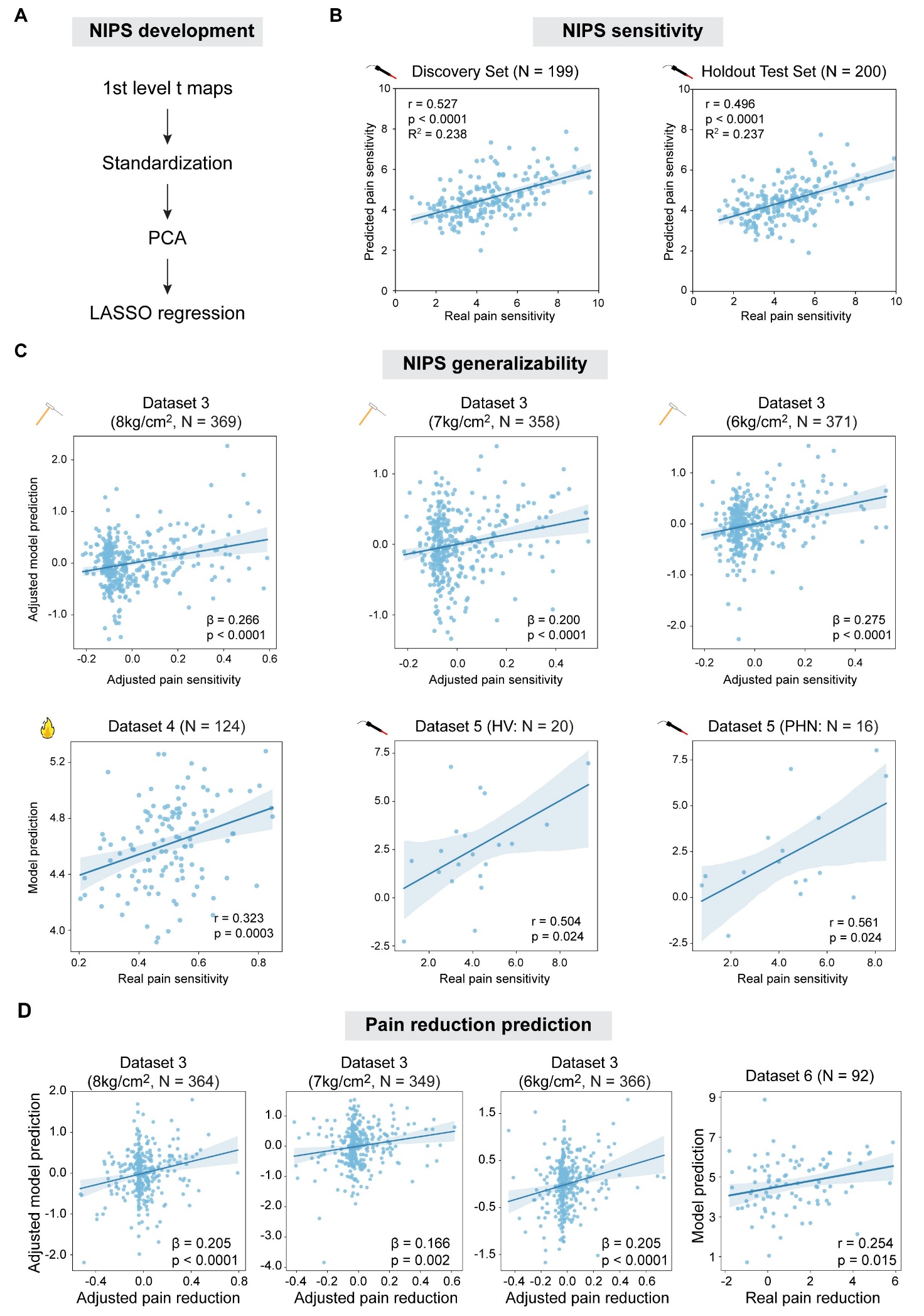
圖4. NIPS模型的高度可泛化性
綜上,這項研究揭示了在樣本量較大的前提下,疼痛誘發腦激活可穩定反映疼痛敏感性個體差異,并開發了一個高度可泛化的疼痛敏感性神經生物標記物。該研究解決了腦激活是否可反映疼痛敏感性這一難題,為客觀量化疼痛敏感性提供了關鍵腦指標,凸顯了大樣本數據結合人工智能算法在解決疼痛基礎研究與臨床應用問題中的重要性。研究結果對基于腦活動的疼痛慢性化早期篩查和開發個體化的疼痛干預手段具有重要啟示意義。
該研究獲得了北京市自然科學基金、國家自然科學基金以及國家重點研發計劃的資助。
相關成果已在線發表于Advanced Science。心理所博士畢業生張立波為論文第一作者,胡理研究員為論文通訊作者。心理所呂雪靖副研究員、張會娟助理研究員、博士畢業生魏朝行、孔亞卓研究員、涂毅恒研究員及意大利技術研究院Giandomenico Iannetti研究員為該研究作出重要貢獻。
論文信息:Zhang, L.-B., Lu, X.-J., Zhang, H.-J., Wei, Z.-X., Kong, Y.-Z., Tu, Y.-H., Iannetti, G.D., and Hu, L*. (2025). A Replicable and Generalizable Neuroimaging-Based Indicator of Pain Sensitivity Across Individuals. Advanced Science, e03373. https://doi.org/10.1002/advs.202503373
相關文獻:
1. Coghill, R.C., McHaffie, J.G., and Yen, Y.-F. (2003). Neural correlates of interindividual differences in the subjective experience of pain. Proceedings of the National Academy of Sciences 100, 8538–8542.
2. Hoeppli, M.E., Nahman-Averbuch, H., Hinkle, W.A., Leon, E., Peugh, J., Lopez-Sola, M., King, C.D., Goldschneider, K.R., and Coghill, R.C. (2022). Dissociation between individual differences in self-reported pain intensity and underlying fMRI brain activation. Nature Communications 13, 3569.
3. Gim, S., Lee, D.H., Lee, S., and Woo, C.-W. (2024). Interindividual differences in pain can be explained by fMRI, sociodemographic, and psychological factors. Nature Communications 15, 7883.
4. Wager, T.D., Atlas, L.Y., Lindquist, M.A., Roy, M., Woo, C.-W., and Kross, E. (2013). An fMRI-based neurologic signature of physical pain. New England Journal of Medicine 368, 1388–1397.
5. Woo, C.-W., Schmidt, L., Krishnan, A., Jepma, M., Roy, M., Lindquist, M.A., Atlas, L.Y., and Wager, T.D. (2017). Quantifying cerebral contributions to pain beyond nociception. Nature Communications 8, 14211.
附件下載:

