心理所研究發現刻畫個體疼痛敏感性的神經指標
疼痛,是一件自然演化贈予人們的最寶貴卻無人想要的禮物。沒有它,人們就失去了最重要的防身利器,極可能在童年就不幸夭折[1];有了它,人們就面臨著潛在的無盡痛楚,甚至有三分之一左右的可能性被慢性疼痛長期折磨[2]。
雖然大多數人都能感受到疼痛,但有些人似乎完全不怕疼,“刮骨療毒”也紋絲不動,而有些人則對疼痛極度敏感,針剛碰到皮膚就痛得直跳。除了日常觀察以外,眾多科學研究也證實了這一點:不同個體對疼痛的敏感性有著極大的差異[3-5]。值得注意的是,怕不怕疼并非是件小事,而是一件具有重大臨床意義的大事。疼痛敏感性個體差異的有效評估對個體止痛藥(如在北美掀起狂風驟雨的阿片類藥物濫用危機)的用量和療效評價等都有著重要的指導意義。
正因如此,疼痛領域多年來一直致力于研究能夠刻畫個體疼痛敏感性差異的神經標記物。然而,以往的研究常常混淆同一個體對不同強度疼痛的感受差異(個體內差異)和不同個體對同一強度疼痛的感受差異(個體間差異),而且研究結果也存在諸多不一致之處。針對這些問題,中國科學院心理健康重點實驗室胡理研究員與倫敦大學學院Giandomenico Iannetti教授合作,采用跨物種研究方法,結合心理物理學測量和電生理技術,發現了高頻γ振蕩信號能可靠且特異地預測個體疼痛敏感性。研究成果已于1月14日在線發表于國際知名期刊美國科學院院刊PNAS[6]。
整個研究由3個不同的實驗組成。實驗1首先招募了96名志愿者(51名女性,年齡21.6 ± 1.7歲),記錄他們在接受不同強度激光熱痛刺激時的疼痛評分及腦電(EEG)數據。為分離疼痛敏感性的個體內差異和個體間差異,研究者將數據分成兩個不同的層次,一是由單個個體對不同疼痛刺激的所有行為評分和腦電響應組成的個體內數據,二是將個體對不同疼痛刺激的行為評分和腦電響應平均后得到的個體間數據。這兩個層次分別對應了個體內差異和個體間差異。
結果顯示,所有由短時激光刺激誘發的EEG響應特征均能較好地反映個體內的疼痛敏感性,包括時域內刺激呈現后120~200 ms內的N1成分、180~300 ms內的N2成分和250~500 ms內的P2成分,以及時頻域內的激光誘發電位(LEP)、低頻α事件相關去同步化(α-ERD)和高頻γ事件相關同步化(γ-ERS),但僅有γ-ERS能刻畫個體間的疼痛敏感性(圖1),且這一結果無法由不同EEG指標的靈敏度差異解釋。進一步的數據分析顯示,高頻γ事件相關同步化能準確預測個體的疼痛敏感性,預測的疼痛評分與真實疼痛評分相關高達0.931(圖2)。
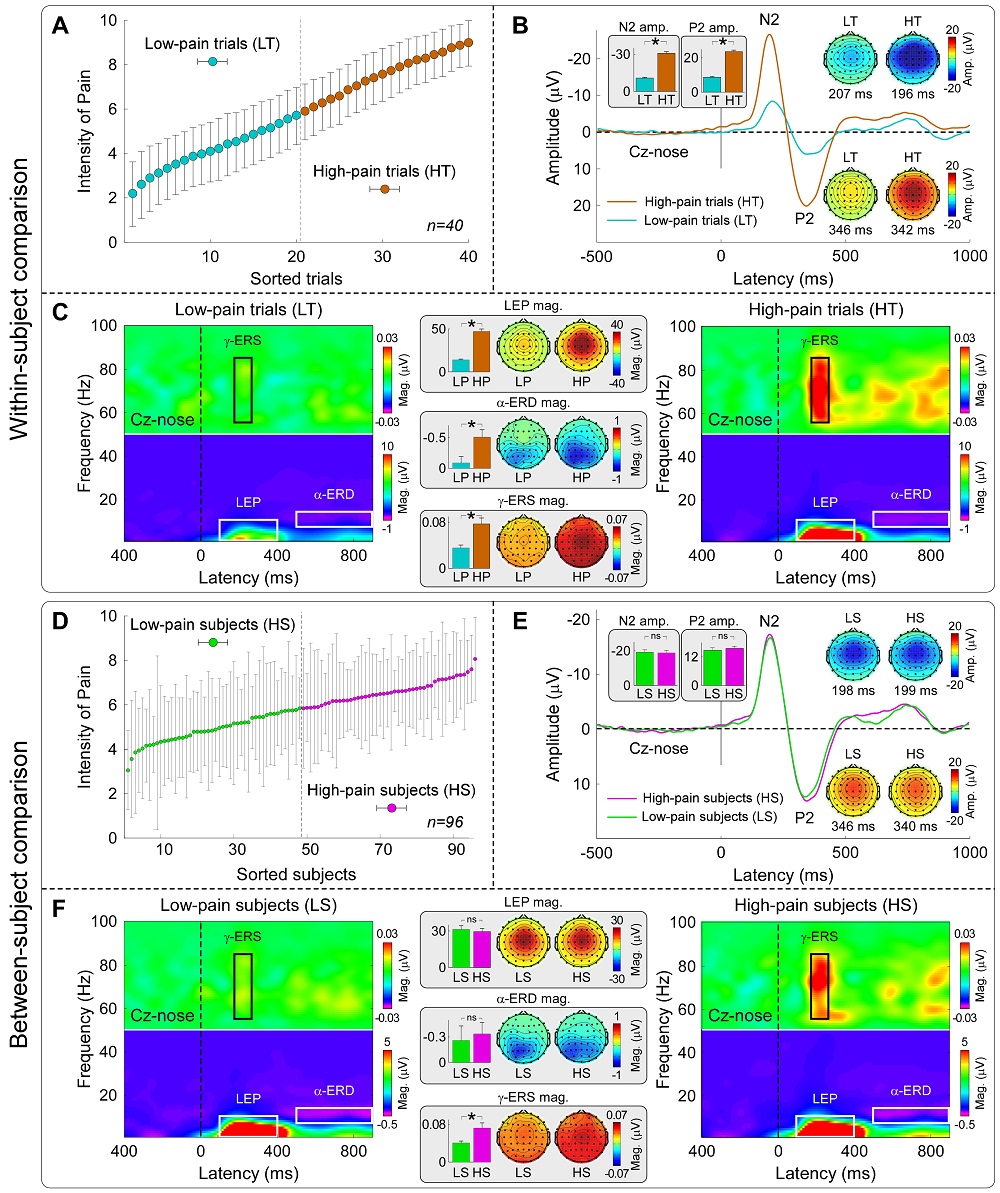
圖 1 個體內和個體間疼痛敏感性預測指標的比較
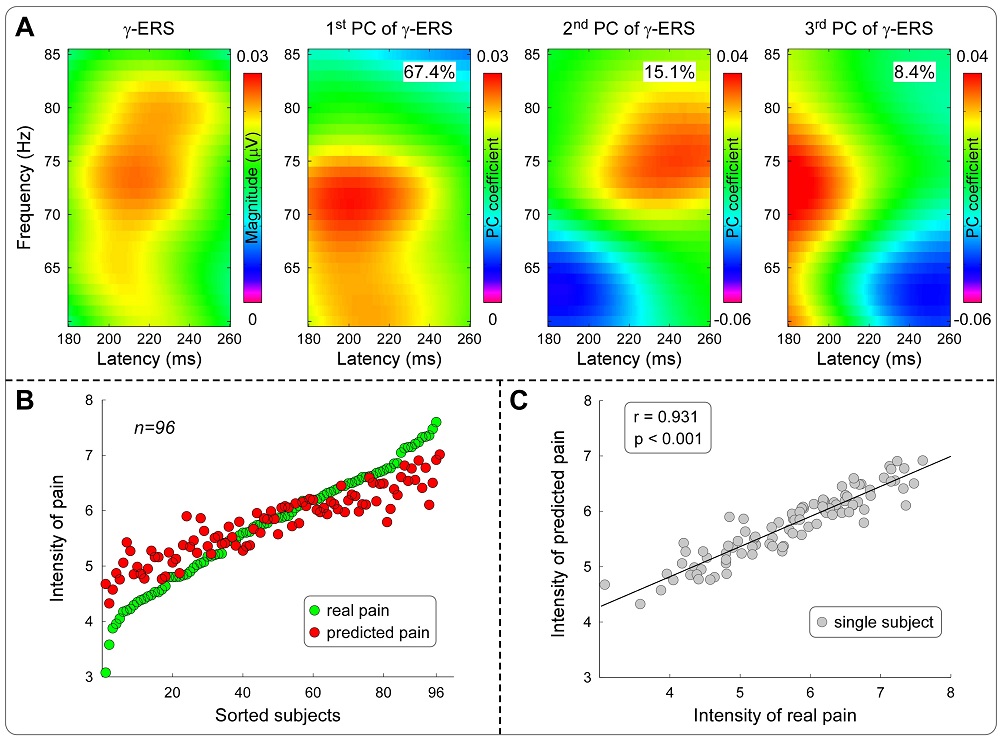
圖 2 γ-ERS準確預測疼痛敏感性的個體差異
由于疼痛刺激具有高凸顯性(saliency),為排除其干擾,實驗2招募了107名志愿者(67名女性,年齡21.6±1.8歲),采集了包含不同強度的視覺、聽覺、觸覺等其它模態短時刺激誘發的EEG信號和相關的心理物理測量數據。結果顯示,γ-ERS無法預測由視覺、聽覺和觸覺刺激引起的個體間感覺強度評分(圖3)。這意味著,刺激凸顯性無法解釋實驗1的研究結果,γ-ERS對感覺敏感性的預測具有疼痛特異性。
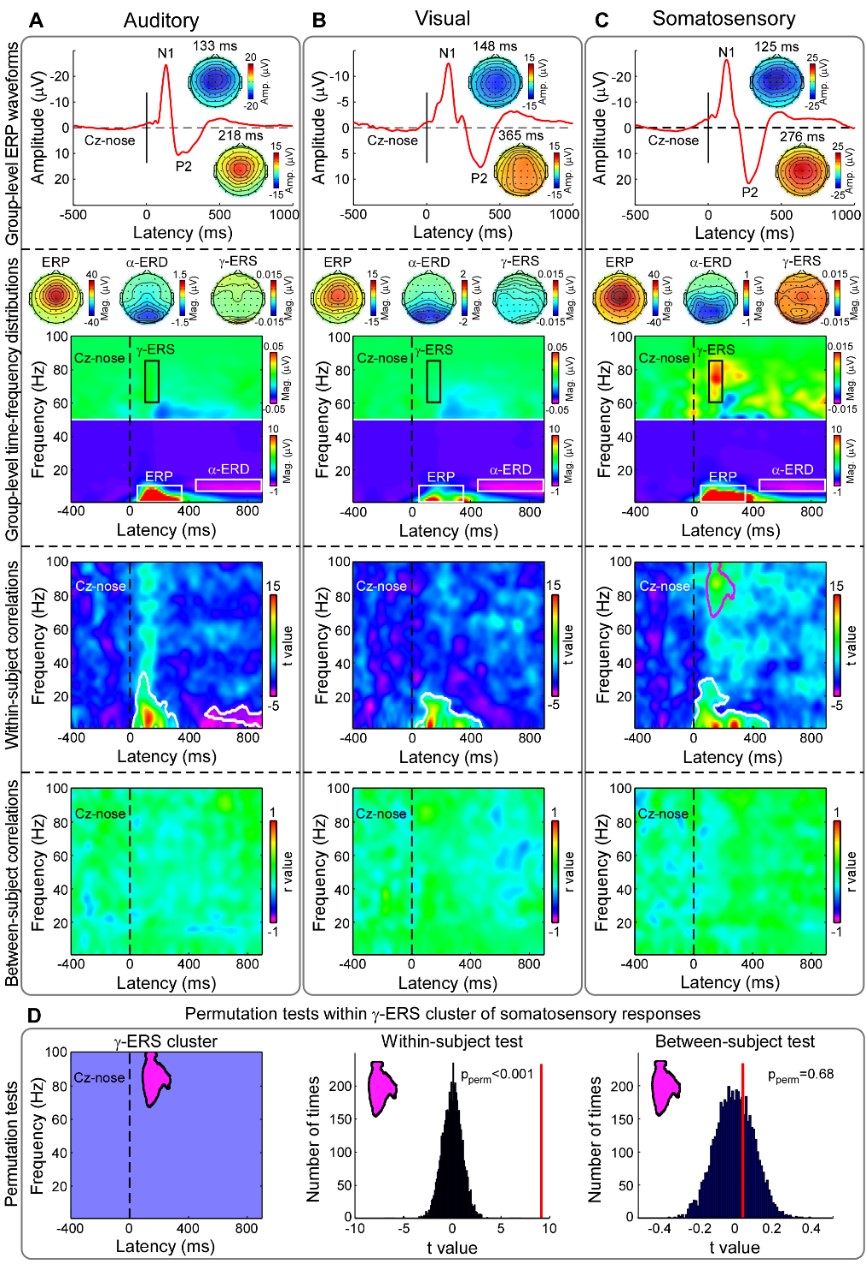
圖 3 多模態感覺刺激誘發EEG腦響應在個體內與個體間差異的比較
實驗1和實驗2均以人類被試為研究對象探究疼痛敏感性個體差異的預測指標。為檢驗γ-ERS預測個體內和個體間疼痛敏感性的特性是否具有跨物種一致性,實驗3進一步采集了來自12只成年雄性Sprague Dawley大鼠的聽覺刺激誘發的顱內腦電響應(ECoG),并將其與胡理研究組之前發表的關于激光誘發γ-ERS與大鼠疼痛行為的研究數據[7]進行了匯總分析。結果與前兩個實驗的結果類似:由激光誘發的大鼠LEP和γ-ERS在個體內水平均與大鼠疼痛行為相關,但僅有γ-ERS在個體間水平與大鼠疼痛行為存在顯著相關(圖4),并且傷害性刺激誘發的γ-ERS的空間地形圖分布與聽覺刺激誘發的γ-ERS存在明顯差異(圖5)。可見,無論在人類還是大鼠身上,γ-ERS均能有效刻畫個體間疼痛敏感性的差異,即具有跨物種的一致性。
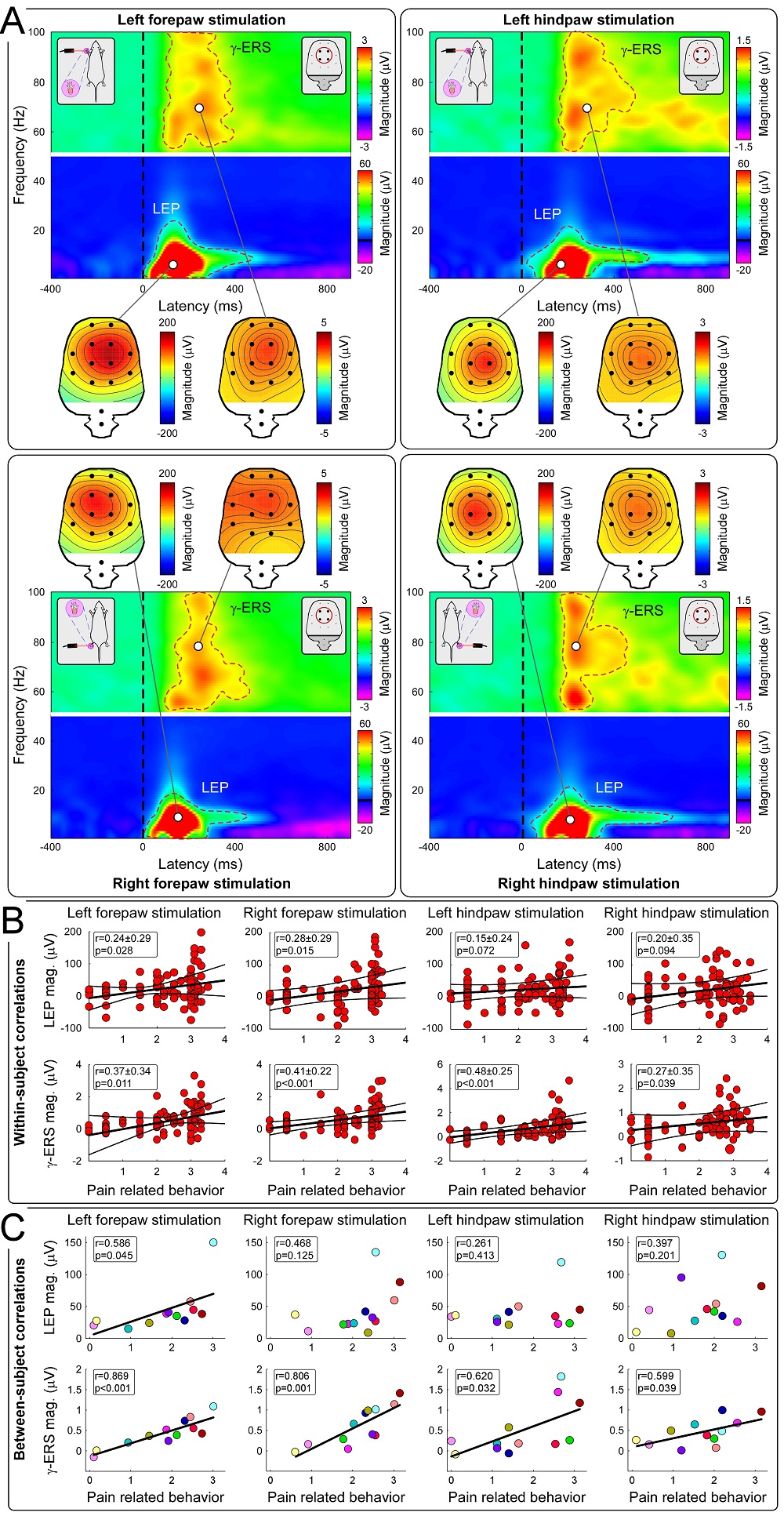
圖 4 ECoG指標反映大鼠疼痛行為的個體內和個體間差異
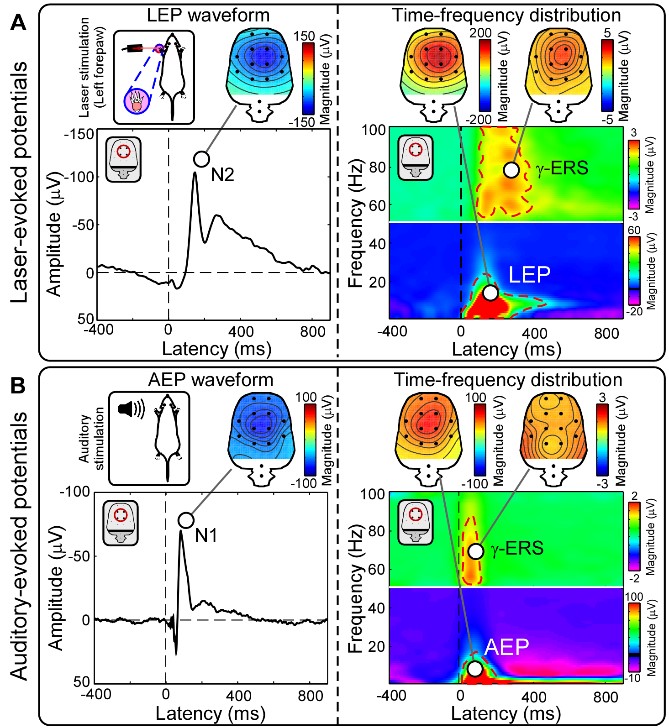
圖 5 痛覺和聽覺刺激誘發大鼠腦響應的差異比較
這些研究結果表明,γ-ERS能特異性地表征個體間疼痛敏感性,不編碼具有同等凸顯性水平的聽覺、視覺和觸覺刺激感覺強度的個體差異,并且該特性在人類和大鼠中具有跨物種一致性。總之,該研究發現了γ-ERS這一編碼個體間疼痛敏感性的神經指標,也加深了人們對疼痛感知覺及其內在機制的理解,并對臨床實踐中如何實現個體化疼痛評估和管理提供了啟示。
該研究受國家自然科學基金委項目(31671141 和 31822025)、中國科學院信息化專項(XXH13506-306)等資助。
論文信息:
Hu*, L., & Iannetti, G. D. (2019). Neural indicators of perceptual variability of pain across species. Proceedings of the National Academy of Sciences, 201812499. https://doi.org/10.1073/pnas.1812499116
論文鏈接:
https://www.pnas.org/content/early/2019/01/08/1812499116
參考文獻:
[1] Nagasako, E. M., Oaklander, A. L., & Dworkin, R. H. (2003). Congenital insensitivity to pain: an update. Pain, 101(3), 213–219. https://doi.org/10.1016/S0304-3959(02)00482-7
[2] Chen, B., Li, L., Donovan, C., Gao, Y., Ali, G., Jiang, Y., … Sun, W. (2016). Prevalence and characteristics of chronic body pain in China: a national study. SpringerPlus, 5, 938. https://doi.org/10.1186/s40064-016-2581-y
[3] Clark, J. W., & Bindra, D. (1956). Individual differences in pain thresholds. Canadian Journal of Psychology/Revue Canadienne de Psychologie, 10(2), 69.
[4] Coghill, R. C., McHaffie, J. G., & Yen, Y.-F. (2003). Neural correlates of interindividual differences in the subjective experience of pain. Proceedings of the National Academy of Sciences, 100(14), 8538–8542.
[5] Nielsen, C. S., Price, D. D., Vassend, O., Stubhaug, A., & Harris, J. R. (2005). Characterizing individual differences in heat-pain sensitivity. Pain, 119(1–3), 65–74.
[6] Hu, L., & Iannetti, G. D. (2019). Neural indicators of perceptual variability of pain across species. Proceedings of the National Academy of Sciences, 201812499. https://doi.org/10.1073/pnas.1812499116
[7] Peng, W., Xia, X., Yi, M., Huang, G., Zhang, Z., Iannetti, G., & Hu, L. (2018). Brain oscillations reflecting pain-related behavior in freely moving rats: Pain, 159(1), 106–118. https://doi.org/10.1097/j.pain.0000000000001069
附件下載:

