心理所研究揭示丘腦特異的疼痛場電位響應信號
疼痛是一種不愉快的感官和情感體驗,保護我們的身體免受實際或潛在的傷害。一方面,疼痛感知同時包含感官辨別信息和情感動機信息,這兩類疼痛信息被認為分別通過大腦外側和內側疼痛通路進行傳遞和處理,丘腦及其皮質連接在這一過程中起著關鍵作用,其響應能夠有效區分疼痛和非疼痛觸覺刺激(Tu et al., 2024)。另一方面,多個丘腦核團被認為是深部腦刺激治療慢性難治性疼痛的有效靶點,現有研究表明調控外側疼痛通路中感覺性丘腦核團的鎮痛效果并不令人滿意,而內側疼痛通路情緒相關靶點的干預或是增強鎮痛療效的有益補充(Meda et al., 2019; You et al., 2022)。然而,當前研究對丘腦的疼痛電生理響應的探索卻十分有限,限制了靶向丘腦閉環神經調控治療神經系統疾病的臨床應用。
近期,中國科學院心理研究所胡理研究組開展了一項動物在體電生理研究(圖1),通過兩個實驗記錄了大鼠的外側疼痛通路(丘腦腹外側核團,ventral posterior lateral nucleus, VPL和初級軀體感覺皮層,primary somatosensory cortex, S1)和內側疼痛通路(丘腦背內側核,medial-dorsal nucleus, MD和前扣帶皮層,anterior cingulate cortex, ACC)的激光誘發腦響應,利用多種電生理信號分析方法揭示了丘腦特異的疼痛場電位響應信號,表現為傷害性激光刺激呈現后約100ms出現的早期負波(early negativity, EN)。相關成果已在線發表于Research,題為Deciphering Authentic Nociceptive Thalamic Responses in Rats。
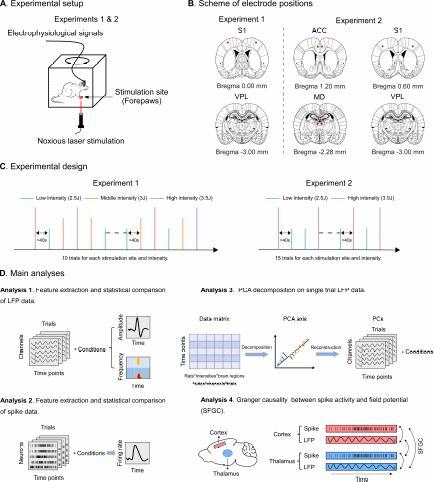
圖1. 實驗設計及主要分析方法
通過上述兩個實驗,獲得了三個關鍵性結果:
其一,雖然丘腦表現出與皮層相似的傷害性誘發神經響應,但同步記錄到的丘腦場電位響應在時間上落后于皮層響應(即時域N1成分)(圖2),這與疼痛通路中信息上傳的時間順序相反,表明丘腦N1響應可能并非起源于丘腦,而是皮層N1信號體積傳導的結果。
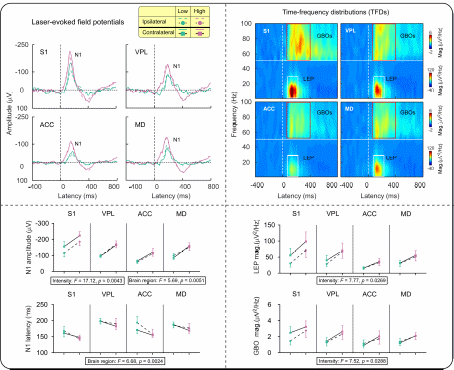
圖2. 丘腦場電位中N1成分的峰值潛伏期顯著晚于皮層N1 成分
其二,主成分分析在丘腦的疼痛場電位響應中揭示了一個獨特的EN成分,該成分在VPL和MD中均可記錄到,其振幅受到疼痛強度的顯著調節,EN的峰值潛伏期顯著短于隨后的N1成分(圖3),表明EN成分可能是丘腦特異的疼痛場電位響應信號。
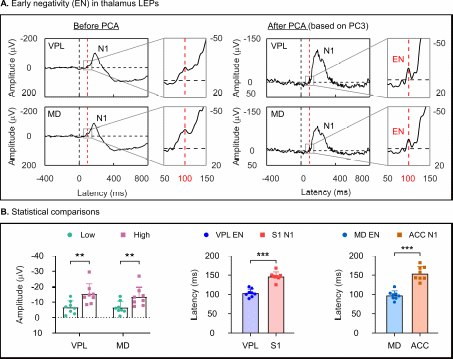
圖3. 丘腦EN成分編碼疼痛強度且峰值潛伏期顯著短于皮層N1 成分
其三,丘腦和皮層之間的峰電位—場電位格蘭杰因果分析(Spike-field Granger causality analysis)提供了支持性證據,丘腦峰電位在100ms左右對皮層場電位信號存在驅動性影響,這與EN的峰值潛伏期接近,并且丘腦到皮層的信息流顯著早于皮層N1成分(圖4)。
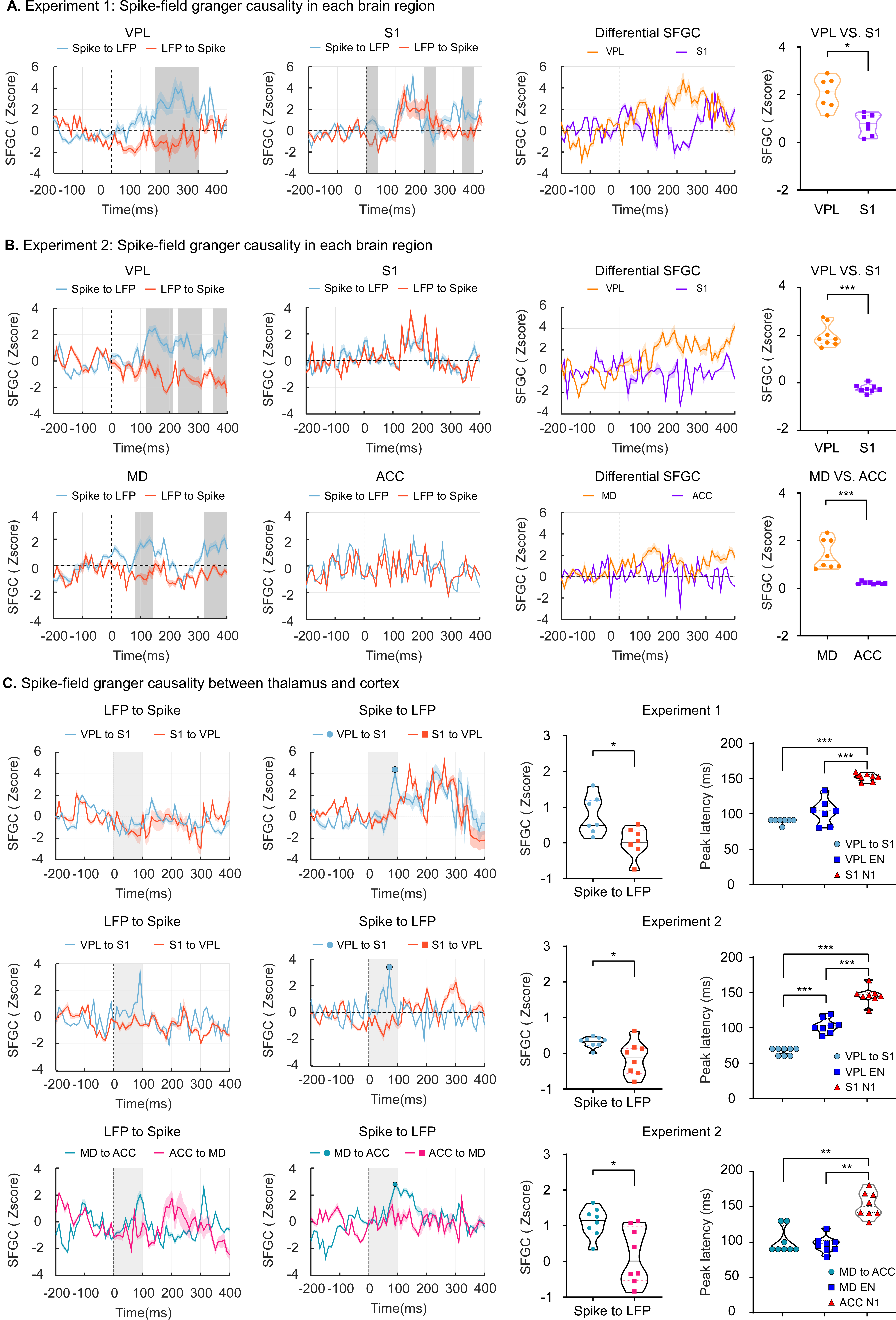
圖4. 丘腦到皮層的信息流顯著早于皮層N1成分
綜上,該研究系統刻畫了丘腦的疼痛電生理響應特征,揭示了丘腦特異的疼痛場電位響應信號,強調了分離真實丘腦神經響應的重要性,有助于更全面地了解丘腦在處理疼痛信息時的功能。此外,鑒于EN成分能夠可靠編碼疼痛強度信息,并且可能是一個普遍的丘腦特征,將EN成分納入閉環神經調控系統實現疼痛的客觀檢測和評估,將有助于優化慢性疼痛的閉環神經調控效果,助力自適應和個性化的疼痛管理。
該研究得到了北京市自然科學基金(JQ22018)、國家自然科學基金項目(32071061)和科技部科技創新2030重大項目(2022ZD0206400)的支持。
論文第一作者為心理所博士生李鎮江,通訊作者為胡理研究員,其他共同作者包括心理所博士生張立波(已畢業)、張峰瑞(已畢業)和助理研究員岳路鵬。
論文信息:
Li, Z., Zhang, L., Zhang, F., Yue, L., & Hu, L.* (2024). Deciphering Authentic Nociceptive Thalamic Responses in Rats. Research. https://spj.science.org/doi/10.34133/research.0348
相關論文:
Tu, Y., Li, Z., Zhang, L., Zhang, H., Bi, Y., Yue, L., & Hu, L. (2024). Pain-preferential thalamocortical neural dynamics across species. Nature human behaviour, 8(1), 149–163.
Meda, K. S., Patel, T., Braz, J. M., Malik, R., Turner, M. L., Seifikar, H., Basbaum, A. I., & Sohal, V. S. (2019). Microcircuit Mechanisms through which Mediodorsal Thalamic Input to Anterior Cingulate Cortex Exacerbates Pain-Related Aversion. Neuron, 102(5), 944–959.e3.
You, H. J., Lei, J., & Pertovaara, A. (2022). Thalamus: The 'promoter' of endogenous modulation of pain and potential therapeutic target in pathological pain. Neuroscience and biobehavioral reviews, 139, 104745.
附件下載:

