心理所研究揭示疼痛敏感性的腦脊網絡預測模型
疼痛的高度主觀性與個體差異既是基礎研究的核心,也是臨床精準鎮痛與閉環神經調控(BCI)實現“解碼—調控—反饋”的關鍵瓶頸。長期以來,現有研究多聚焦于“大腦中心”而忽視了脊髓作為關鍵關口的重要作用,且缺乏對運動皮層鎮痛網絡機制及脊髓耦合關系量化指標。因此,研究團隊將研究視角拓展至“皮層-腦干-脊髓”全神經軸,旨在通過構建可泛化的疼痛敏感性解碼模型,并結合運動皮層定向擾動,確立可操作、可推廣的客觀指標,從而實現從狀態解碼到因果調控的閉環驗證。
中國科學院心理研究所孔亞卓研究組聯合多家單位開展了一項研究,利用先進的皮層-脊髓同步功能磁共振成像(Corticospinal fMRI)技術,在6個健康人數據集和2個臨床數據集上開發了一種全新的神經標志物——“皮層-脊髓疼痛敏感性標志物”(Corticospinal pain sensitivity signature, CSps)。該研究首次將大腦和脊髓作為一個整合的系統,揭示了皮層-脊髓功能連接模式在預測個體疼痛敏感性及臨床疼痛中的重要作用。
該研究首先基于健康參與者的靜息態皮層-脊髓功能連接數據,結合機器學習算法構建了CSps模型。研究發現,CSps能夠準確預測個體的熱痛閾值,并在多個獨立的外部數據集中表現出優異的泛化能力(圖1a-c)。此外,該模型具有良好的疼痛特異性,能夠有效區分疼痛與非疼痛(如冷感覺)的神經反應(圖1e),且不受個體焦慮、抑郁等心理因素及人口學變量的影響(圖1d)。
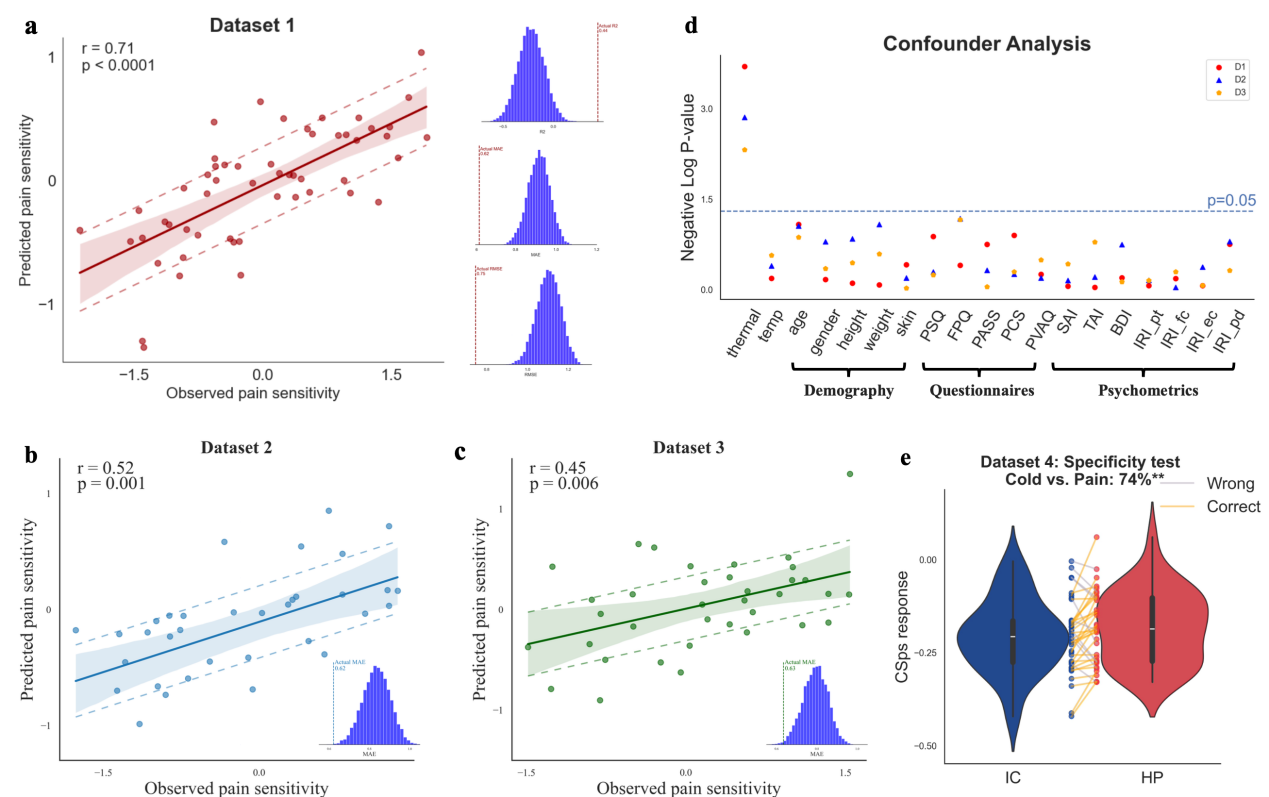
圖1. CSps的預測效果
在臨床應用驗證中,研究者將CSps模型應用于兩類不同病因的臨床疼痛患者群體——亞急性期帶狀皰疹疼痛(ZAP)和糖尿病伴隨慢性疼痛(DMC)。結果顯示,基于健康人數據訓練的CSps模型能夠成功預測這兩類患者的臨床疼痛評分(圖2a),且預測性能顯著優于傳統的僅基于腦部數據的模型或僅基于脊髓數據的模型(圖2c)。這表明,整合了腦與脊髓信息的神經標志物能夠捕捉到更核心的疼痛處理機制,架起了實驗室疼痛測量與臨床患者癥狀之間的橋梁。
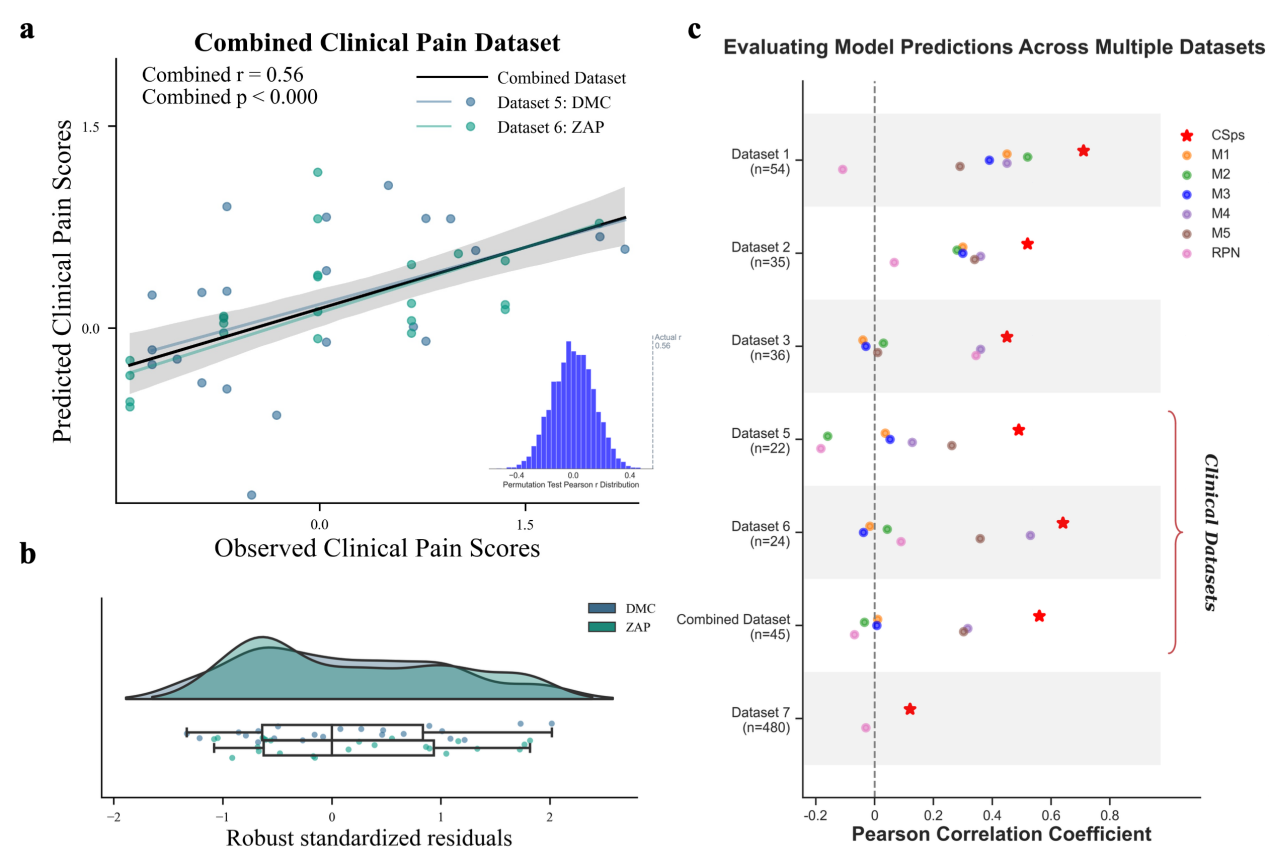
圖2. CSps模型在慢性疼痛患者中的預測效果及與其他模型的比較
從模型結構看,CSps由一組稀疏連接構成,其中最突出的正向預測通路之一,是運動皮層與頸髓C4腹角之間的連接,形成一條“從皮層到脊髓的縱向整合軸”。基于這一模型指向性證據,研究團隊進一步設計了關鍵的“調控-反饋”環節:在經偽刺激對照的10 Hz重復經顱磁刺激(rTMS)實驗中,對M1進行定向擾動,并在刺激前后采集皮層-脊髓靜息態成像及疼痛任務數據。結果顯示,在真實M1刺激組中,CSps評分變化與疼痛感知變化顯著相關(r=0.55),而偽刺激組不顯著(圖3d-e);同時,運動區-脊髓關鍵連接也出現與刺激相關的改變(圖3c)。
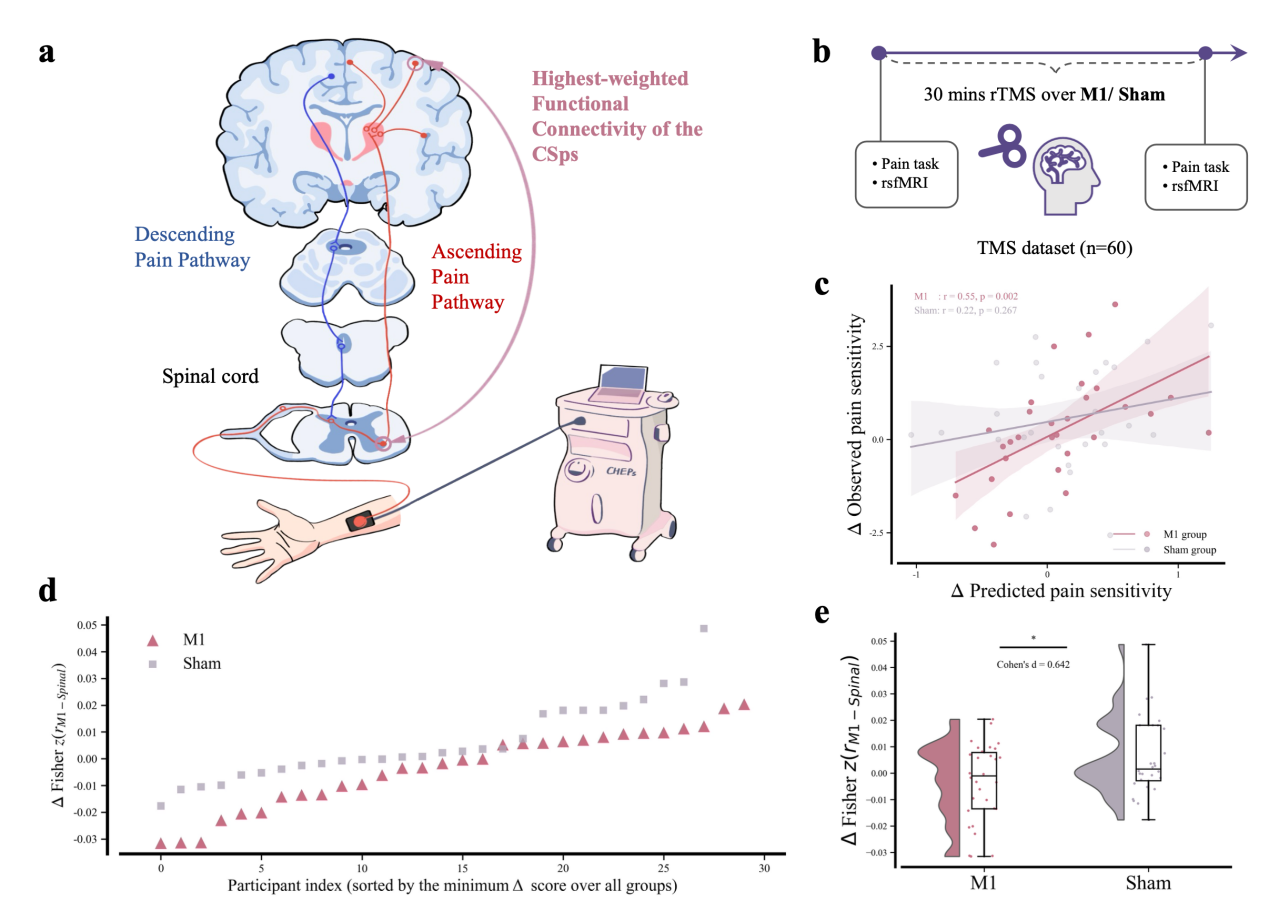
圖3. rTMS干預揭示M1-脊髓連接與疼痛感知的因果聯系
綜上所述,該研究開發了一種基于皮層-脊髓功能連接的神經標志物CSps。CSps提供了一個以神經軸連接模式為基礎、可量化的“疼痛相關表征”,有望與更高時間分辨率的腦電/肌電/植入式信號等結合,推動對疼痛意識狀態的實時解碼與分型。未來,通過實時監測CSps信號波動,結合閉環神經調控技術,有望實現對慢性疼痛患者的精準、即時干預,讓“腦機接口止痛”成為可能。
該研究受到國家自然科學基金(82441056, 82071883, 82371937)、國家重點研發計劃(2022YFC3500603)及北京市自然科學基金(IS23108)等項目的資助。
該研究成果已在線發表于Nature Communications。心理所博士生林校民為論文第一作者,心理所孔亞卓研究員、山東省立醫院郭凌飛主任、首都醫科大學宣武醫院倪兵副主任、重慶大學附屬腫瘤醫院張久權主任、首都醫科大學天壇醫院劉亞歐主任為共同通訊作者。此外,心理所胡理研究員、利物浦大學Jonathan C. W. Brooks教授、達特茅斯學院Tor D. Wager教授以及牛津大學Irene Tracey教授等合作者,在研究設計、數據解釋及論文修訂方面也做出了重要貢獻。
論文信息:Lin, X.-M., Guo, L.-F., Ni, B., et al. (2025). A corticospinal signature for interindividual pain sensitivity. Nature Communications. https://doi.org/10.1038/s41467-025-67132-6
附件下載:

